 Реклама Google — средство выживания форумов :)
Реклама Google — средство выживания форумов :)
-
![[image]](https://www.balancer.ru/cache/sites/net/tw/twirpx/cv01/0122/128x128-crop/0122290.jpg)
Синтез хлоратов и перхлоратов
Теги:
Xan> Кстати, о кристаллизации.
У меня перед кристаллизацией ещё будет анализ на готовность. Это время уже скоро придет. Буду мучить вопросами конечно после очередного прочтения того что ты писал раньше на эту тему. Я всю твою информацию по хлорату за год копировал в ворд и сохранял, чтобы потом не искать.
У меня перед кристаллизацией ещё будет анализ на готовность. Это время уже скоро придет. Буду мучить вопросами конечно после очередного прочтения того что ты писал раньше на эту тему. Я всю твою информацию по хлорату за год копировал в ворд и сохранял, чтобы потом не искать.

LEVSHA> Я же не про свой вариант. Non-conformist собирается использовать полулитровую банку. Вот я и говорю, что это только грязь разводить.
Откуда такая информация? Я планирую три трёхлитровые банки, и корпуса анодов соответствующей длины под них уже заготовил! Может, про пол-литровую я писал - так это же просто проба герметичности крышки была, )) пол-литровка случайно на работе нашлась, с болтиками!
Откуда такая информация? Я планирую три трёхлитровые банки, и корпуса анодов соответствующей длины под них уже заготовил! Может, про пол-литровую я писал - так это же просто проба герметичности крышки была, )) пол-литровка случайно на работе нашлась, с болтиками!

Non-conformist>> трёхлитровые банки
Xan> Ну вот многовато, на мой взгляд.
Три штуки многовато, или три литра? А сколько и какие банки ты имел в виду, говоря о непрерывном процессе?
Xan> Ну вот многовато, на мой взгляд.
Три штуки многовато, или три литра? А сколько и какие банки ты имел в виду, говоря о непрерывном процессе?

Non-conformist> Откуда такая информация? Я планирую три трёхлитровые банки.

Жадный ты до «добра».

Жадный ты до «добра».


Xan> .
В начале процесса почти весь раствор был матовый от пузырьков через неделю матовой была только верхняя половина .Сейчас раствор совершенно прозрачный, то есть пузырьки от электродов идут а раствор прозрачный
Вопрос к чему это!?
В начале процесса почти весь раствор был матовый от пузырьков через неделю матовой была только верхняя половина .Сейчас раствор совершенно прозрачный, то есть пузырьки от электродов идут а раствор прозрачный
Вопрос к чему это!?

LEVSHA> Жадный ты до «добра». 
Отнюдь. В случае успеха планирую безвозмездно (за символическое вознаграждение) одаривать излишками эликсира молодости всех надёжных (в смысле квалификации и благих намерений) заинтересованных лиц, компактно проживающих в моём регионе. )) На мой взгляд, доступный источник практически бесплатного сабжа подстегнёт любительские исследования в нужном мне направлении.
зы: Да, а вообще сколько дают за это дело сейчас? В смысле срока? ))

Отнюдь. В случае успеха планирую безвозмездно (за символическое вознаграждение) одаривать излишками эликсира молодости всех надёжных (в смысле квалификации и благих намерений) заинтересованных лиц, компактно проживающих в моём регионе. )) На мой взгляд, доступный источник практически бесплатного сабжа подстегнёт любительские исследования в нужном мне направлении.
зы: Да, а вообще сколько дают за это дело сейчас? В смысле срока? ))

Non-conformist> зы: Да, а вообще сколько дают за это дело сейчас? В смысле срока? ))
Из истории, почему нельзя посадить грека – потому что он не признается.
Из истории, почему нельзя посадить грека – потому что он не признается.

Xan> Три литра многовато. Обрабатываемая порция плохо помещается в обычную посуду.
Ну, тогда будем искать подходящие эмалированные кастрюли или пластиковые вёдра. Аноды переделывать уже не буду, а регулировать глубину их погружения можно лишь ограниченно, ± миллиметров по тридцать в каждую сторону максимум. Дальше не пускают стыки - трубки-то из кусочков спаяны. Всё рассчитано на 200 мм - высоту банки минус 30 мм над днищем.
Хотя, может и для двухлитровых подойдут - может следующее (через стык) коленце как раз на плоскость крышки придётся... Надо будет померить.
Ну, тогда будем искать подходящие эмалированные кастрюли или пластиковые вёдра. Аноды переделывать уже не буду, а регулировать глубину их погружения можно лишь ограниченно, ± миллиметров по тридцать в каждую сторону максимум. Дальше не пускают стыки - трубки-то из кусочков спаяны. Всё рассчитано на 200 мм - высоту банки минус 30 мм над днищем.
Хотя, может и для двухлитровых подойдут - может следующее (через стык) коленце как раз на плоскость крышки придётся... Надо будет померить.

Граждане химики помогите расшифровать картинку.
Решил проверить электролит на содержание хлорида. Пока нитрат серебра использовать не стал(жаба). Сделал раствор нитрата свинца 3.3гр. на 10мл. воды. Из электролизёра сделал забор электролита, прокипятил, долил воды до первоначального объема плотность примерно 1.3 предположительный состав на один литр 20-100 гр. хлорида натрия 300-400 хлората натрия и 2гр. калий двухромовокислый а также следы кальция.
Два гр. электролита поместил в пробирку и по каплям в течении минуты добавил ~ 0.4мл. раствора нитрата свинца. Вот что получилось фото сделано через 3-4мин.
Решил проверить электролит на содержание хлорида. Пока нитрат серебра использовать не стал(жаба). Сделал раствор нитрата свинца 3.3гр. на 10мл. воды. Из электролизёра сделал забор электролита, прокипятил, долил воды до первоначального объема плотность примерно 1.3 предположительный состав на один литр 20-100 гр. хлорида натрия 300-400 хлората натрия и 2гр. калий двухромовокислый а также следы кальция.
Два гр. электролита поместил в пробирку и по каплям в течении минуты добавил ~ 0.4мл. раствора нитрата свинца. Вот что получилось фото сделано через 3-4мин.
Прикреплённые файлы:
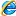

Та же пробирка через 25мин.
Прикреплённые файлы:
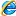

Xan> На фильтр, промыть, высушить, взвесить, посчитать.
Скажем так, я ждал другого ответа, а нет никого.
Скажем так, я ждал другого ответа, а нет никого.

Xan>> На фильтр, промыть, высушить, взвесить, посчитать.
LEVSHA> Скажем так, я ждал другого ответа, а нет никого.
Ну там ничего, кроме хлористого свинца выпась не могло.
Ну, чуть-чуть хромата свинца.
Поэтому взвесив осадок можно количественно определить содержание иона хлора.
Растворимость хлористого свинца около 1 г / 100 г воды.
То есть, примерно 0.25 г хлора на 100 г воды — нижний предел определения.
LEVSHA> Скажем так, я ждал другого ответа, а нет никого.
Ну там ничего, кроме хлористого свинца выпась не могло.
Ну, чуть-чуть хромата свинца.
Поэтому взвесив осадок можно количественно определить содержание иона хлора.
Растворимость хлористого свинца около 1 г / 100 г воды.
То есть, примерно 0.25 г хлора на 100 г воды — нижний предел определения.


LEVSHA> Граждане химики помогите расшифровать картинку.
А в чём вопрос? Кристаллы укрупнились при стоянии, более полно выпали.
Но ты зря используешь такой концентрированный раствор. Неизвестно, может хлорат свинца тоже выпадает. А может и нитрат натрия, посчитай.
Что ты собирался делать с этим осадком? Как считать хлорид?
А в чём вопрос? Кристаллы укрупнились при стоянии, более полно выпали.
Но ты зря используешь такой концентрированный раствор. Неизвестно, может хлорат свинца тоже выпадает. А может и нитрат натрия, посчитай.
Что ты собирался делать с этим осадком? Как считать хлорид?


Xan> Ну там ничего, кроме хлористого свинца выпась не могло.
Xan> Ну, чуть-чуть хромата свинца.
Я так тоже думал но что-то не так разбираюсь.
Xan> Ну, чуть-чуть хромата свинца.
Я так тоже думал но что-то не так разбираюсь.

Serge77> Но ты зря используешь такой концентрированный раствор.
Сто процентов согласен, но это как говорится проба пера + хлорид синца не серебра.
Serge77> А в чём вопрос? Кристаллы укрупнились при стоянии, более полно выпали.
. Изначально основной вопрос был в том, почему три разных слоя и что это такое.
2.Откуда такие кристаллы, если раствора 2мл. А растворимость хлорида свинца ~0.9г на 100г воды при комнатной температуре.
3. Что такое желтый осадок, если это реакция с хроматом, то почему его так много ведь в 2мл моего раствора его примерно 4мГ.
4. При нагреве пробирки до кипения весь белый осадок растворился и остался только желтый растворимость хлорида свинца 3,25 г/100 г (100°). После остывания выросли прозрачные игольчатые кристаллы.
В общем, я в этом вопросе слаб и мне не совсем понятно.
Буду делать раствор нитрата серебра и попробую реакцию с малыми концентрациями.
Serge77> Неизвестно, может хлорат свинца тоже выпадает.
Serge77> А может и нитрат натрия, посчитай.
Я это точно не знаю потому и спрашиваю.
Serge77> Что ты собирался делать с этим осадком? Как считать хлорид?
Изначально собирался прикапывать нитрат пока перестанет мутнеть раствор а потом исходя из количества электролита и использованного нитрата посчитать хлорид.
Сто процентов согласен, но это как говорится проба пера + хлорид синца не серебра.
Serge77> А в чём вопрос? Кристаллы укрупнились при стоянии, более полно выпали.
. Изначально основной вопрос был в том, почему три разных слоя и что это такое.
2.Откуда такие кристаллы, если раствора 2мл. А растворимость хлорида свинца ~0.9г на 100г воды при комнатной температуре.
3. Что такое желтый осадок, если это реакция с хроматом, то почему его так много ведь в 2мл моего раствора его примерно 4мГ.
4. При нагреве пробирки до кипения весь белый осадок растворился и остался только желтый растворимость хлорида свинца 3,25 г/100 г (100°). После остывания выросли прозрачные игольчатые кристаллы.
В общем, я в этом вопросе слаб и мне не совсем понятно.
Буду делать раствор нитрата серебра и попробую реакцию с малыми концентрациями.
Serge77> Неизвестно, может хлорат свинца тоже выпадает.
Serge77> А может и нитрат натрия, посчитай.
Я это точно не знаю потому и спрашиваю.
Serge77> Что ты собирался делать с этим осадком? Как считать хлорид?
Изначально собирался прикапывать нитрат пока перестанет мутнеть раствор а потом исходя из количества электролита и использованного нитрата посчитать хлорид.
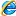

Это сообщение редактировалось 08.06.2012 в 04:04
Решил процесс добить до конца, иначе все равно бы не заснул.
Так вот нитрат свинца это полная туфта, а вот нитрат серебра просто сказка.
Прочес произошел точно, так как говорил Serge77 сначала выпал хлорид, а потом хромат.
Фото последняя капля.
Так вот нитрат свинца это полная туфта, а вот нитрат серебра просто сказка.
Прочес произошел точно, так как говорил Serge77 сначала выпал хлорид, а потом хромат.
Фото последняя капля.
Прикреплённые файлы:
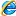

Фото осадок после отстаивания.
Прикреплённые файлы:
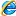

Решил для контроля довести до кипения осадок хромата исчез. Когда раствор остыл, еще капнул нитрата серебра фото. Только цвет стал другой.
Прикреплённые файлы:
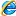

LEVSHA> 4. При нагреве пробирки до кипения весь белый осадок растворился и остался только желтый растворимость хлорида свинца 3,25 г/100 г (100°). После остывания выросли прозрачные игольчатые кристаллы.
Разбавить, всё легко растворимое растворится.
Надо, чтоб хлорида свинца осталось немного в осадке, чтоб его количество определить, а всё остальное растворилось.
А потом растворённый хлорид свинца, зная его растворимость, можно учесть по количеству раствора и воды для промывки.
Можно даже просто добавлять воды, пока весь хлорид свинца не растворится, а потом по объёму раствора посчитать, сколько его было.
Разбавить, всё легко растворимое растворится.
Надо, чтоб хлорида свинца осталось немного в осадке, чтоб его количество определить, а всё остальное растворилось.
А потом растворённый хлорид свинца, зная его растворимость, можно учесть по количеству раствора и воды для промывки.
Можно даже просто добавлять воды, пока весь хлорид свинца не растворится, а потом по объёму раствора посчитать, сколько его было.


 Реклама Google — средство выживания форумов :)
Реклама Google — средство выживания форумов :)
***
А что будет, если на каком-либо этапе электролиза пропадёт питание? Пойдёт ли обратный процесс (восстановления)? Имею в виду электродную пару "платина / свинец".
А что будет, если на каком-либо этапе электролиза пропадёт питание? Пойдёт ли обратный процесс (восстановления)? Имею в виду электродную пару "платина / свинец".

Copyright © Balancer 1997..2023
Создано 17.04.2012
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
Создано 17.04.2012
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
 LEVSHA
LEVSHA

 инфо
инфо инструменты
инструменты
 Xan
Xan







