-
![[image]](https://www.balancer.ru/cache/images/forums/logos/1358/128x128-crop/1358642-boychemist-290x300.jpg)
Вопрос возник: электроосаждение иридия из расплава солей
Теги:
au> Надо как-то наши физики синхронизировать. 
au> 1. В расплаве NaCl присутствует хлор, кислорода там нет.
Просьба различать хлор (газ, Cl2) и хлорид-анион Cl-1 ! Газообразный хлор - страшный яд и окислитель, хлорид-анион в составе того же NaCl каждый употребляет в достаточных количествах и не окисляется.
Так же и металлический натрий при контакте с водой воспламеняется, а поваренная соль, содержащая катион Na+1 еще ни разу не загорелась.
au> 2. Про плёнку оксида на поверхности иридия — это откуда взялось? ...
au> ... At elevated temperatures of about 600°C, iridium metal combines with oxygen to form a coating of iridium dioxide, IrO2.
Собственно, в вопросе содержится ответ.
au> Из этого можно предположить, что в расплаве (800~1000C) NaCl иридий в контакте с хлором может ионизироваться (800>>600), и раствориться в расплаве.
При этих условиях (при контакте с газообразным хлором при 800°C) иридий будет "ионизироваться", т.е. превращаться из металла в хлорид и без NaCl.
au> Хлорид образоваться не сможет, потому что разваливается.
IrCl3 разваливается,а образуется в этих условиях IrCl4.
au> 1. В расплаве NaCl присутствует хлор, кислорода там нет.
Просьба различать хлор (газ, Cl2) и хлорид-анион Cl-1 ! Газообразный хлор - страшный яд и окислитель, хлорид-анион в составе того же NaCl каждый употребляет в достаточных количествах и не окисляется.
Так же и металлический натрий при контакте с водой воспламеняется, а поваренная соль, содержащая катион Na+1 еще ни разу не загорелась.
au> 2. Про плёнку оксида на поверхности иридия — это откуда взялось? ...
au> ... At elevated temperatures of about 600°C, iridium metal combines with oxygen to form a coating of iridium dioxide, IrO2.
Собственно, в вопросе содержится ответ.
au> Из этого можно предположить, что в расплаве (800~1000C) NaCl иридий в контакте с хлором может ионизироваться (800>>600), и раствориться в расплаве.
При этих условиях (при контакте с газообразным хлором при 800°C) иридий будет "ионизироваться", т.е. превращаться из металла в хлорид и без NaCl.
au> Хлорид образоваться не сможет, потому что разваливается.
IrCl3 разваливается,а образуется в этих условиях IrCl4.
Это сообщение редактировалось 24.07.2007 в 01:33
Serge77>>>Несмотря на то, что пишут "is attacked by molten salts, such as NaCl and NaCN".
Serge77>> Однако здесь про хлор ничего не написано. Потому что хлора там нет. А есть хлорид-анион. Который с иридием никак не реагирует.
au> У меня большая к вам просьба писать тут только факты или достоверные данные. Если в 85 издании написано что иридий растворяется в расплаве NaCl и NaCN, и LANL это себе посимвольно скопировал, а вы заявляете что это не так, не представляя никаких фактов или достоверных данных, то верить вашему заявлению нет никакой причины. Я тут пытаюсь собрать достоверную информацию, которой очень мало, и прошу мне помочь в этом тех кто может это сделать.
Золото тоже растворяется в растворе NaCN. Однако, только в присутствии кислорода воздуха. Сверхтонкой пленки оксидов на поверхности золота достаточно для образования цианидных комплексов, растворимых в воде. Этот метод используется в промышленности при добыче золота из бедных месторождений.
Serge77>> Однако здесь про хлор ничего не написано. Потому что хлора там нет. А есть хлорид-анион. Который с иридием никак не реагирует.
au> У меня большая к вам просьба писать тут только факты или достоверные данные. Если в 85 издании написано что иридий растворяется в расплаве NaCl и NaCN, и LANL это себе посимвольно скопировал, а вы заявляете что это не так, не представляя никаких фактов или достоверных данных, то верить вашему заявлению нет никакой причины. Я тут пытаюсь собрать достоверную информацию, которой очень мало, и прошу мне помочь в этом тех кто может это сделать.
Золото тоже растворяется в растворе NaCN. Однако, только в присутствии кислорода воздуха. Сверхтонкой пленки оксидов на поверхности золота достаточно для образования цианидных комплексов, растворимых в воде. Этот метод используется в промышленности при добыче золота из бедных месторождений.
ad2> Необходимость использования для электролиза расплавов солей, а не их водных растворов, обычно связана с необходимостью высоких плотностей токов и, соответственно, значений потенциалов. В этом плане стеклоуглерод не лучший выбор, скажем в водных растворах, если не смотреть в справочники, он при потенциалах выше 1,4-1,5 В (н.в.э.) окисляется. В расплавах потенциалы выше и, скорее всего, стеклоуглеродный тигель в качестве анода будет окисляться до CCl4, COCl2 и т.п. Все-таки лучше использовать графит, его не так жалко. Лично я бы взял графитовый тигель в качестве катода и графитовый же электрод (отработанный на каком-нибудь спектральном приборе (где используется искра, дуга и т.п.), и не нужно ничего платить и высокая чистота) в качестве анода.
Если посмотреть на исходный вопрос, становится понятно, что задача - не просто выделение иридия, а получение детали (сола реактивного двигателя) из компактного металла гальванопластикой, т.к. другие способы получения таких деталей - малотехнологичны (прессование иридиевой губки).
Вероятно, целесообразным будет использование стеклоуглеродного катода (точная форма/размер изделия) и иридиевого анода.
ad2> Иридиевый анод в данном случае ни к чему, потенциал окисления иридия высок и потребуются дополнительные затраты энергии на его растворение.
Потенциал окисления высок, но не выше потенциала восстановления! На катоде-то иридий при этом потенциале восстанавливается до металла - а значит на аноде будет окисляться до катиона!
Если посмотреть на исходный вопрос, становится понятно, что задача - не просто выделение иридия, а получение детали (сола реактивного двигателя) из компактного металла гальванопластикой, т.к. другие способы получения таких деталей - малотехнологичны (прессование иридиевой губки).
Вероятно, целесообразным будет использование стеклоуглеродного катода (точная форма/размер изделия) и иридиевого анода.
ad2> Иридиевый анод в данном случае ни к чему, потенциал окисления иридия высок и потребуются дополнительные затраты энергии на его растворение.
Потенциал окисления высок, но не выше потенциала восстановления! На катоде-то иридий при этом потенциале восстанавливается до металла - а значит на аноде будет окисляться до катиона!
ad2> Необходимость использования для электролиза расплавов солей, а не их водных растворов, обычно связана с необходимостью высоких плотностей токов и, соответственно, значений потенциалов. В этом плане стеклоуглерод не лучший выбор, скажем в водных растворах, если не смотреть в справочники, он при потенциалах выше 1,4-1,5 В (н.в.э.) окисляется. В расплавах потенциалы выше и, скорее всего, стеклоуглеродный тигель в качестве анода будет окисляться до CCl4, COCl2 и т.п. Все-таки лучше использовать графит, его не так жалко. Лично я бы взял графитовый тигель в качестве катода и графитовый же электрод (отработанный на каком-нибудь спектральном приборе (где используется искра, дуга и т.п.), и не нужно ничего платить и высокая чистота) в качестве анода.
Если посмотреть на исходный вопрос, становится понятно, что задача - не просто выделение иридия, а получение детали (сопла реактивного двигателя) из компактного металла гальванопластикой, т.к. другие способы получения таких деталей - малотехнологичны (прессование иридиевой губки).
Вероятно, целесообразным будет использование стеклоуглеродного катода (точная форма/размер изделия) и иридиевого анода.
ad2> Иридиевый анод в данном случае ни к чему, потенциал окисления иридия высок и потребуются дополнительные затраты энергии на его растворение.
Потенциал окисления высок, но не выше потенциала восстановления! На катоде-то иридий при этом потенциале восстанавливается до металла - а значит на аноде будет окисляться до катиона!
Если посмотреть на исходный вопрос, становится понятно, что задача - не просто выделение иридия, а получение детали (сопла реактивного двигателя) из компактного металла гальванопластикой, т.к. другие способы получения таких деталей - малотехнологичны (прессование иридиевой губки).
Вероятно, целесообразным будет использование стеклоуглеродного катода (точная форма/размер изделия) и иридиевого анода.
ad2> Иридиевый анод в данном случае ни к чему, потенциал окисления иридия высок и потребуются дополнительные затраты энергии на его растворение.
Потенциал окисления высок, но не выше потенциала восстановления! На катоде-то иридий при этом потенциале восстанавливается до металла - а значит на аноде будет окисляться до катиона!
Народ, прошу придерживаться конкретных условий, потому что интересует только условия с расплавом. То есть про кислород и оксидные плёнки писать не надо — нет там нигде кислорода: ни в расплаве соли, ни в аргоне вокруг него, ни на самом металле. Это условия.
Насчёт стеклографитового тигля. Именно такой применялся во многих экспериментах с электролизом в расплавах NaCl и NaCl/KCl, потому и привлёк внимание. Конкретно вот пример, где стеклографитовый тигель был анодом при электроосаждении урана из UCl3 при 670-710C, и катод тоже был стеклографитовый. Стеклографит и просто графит — это вовсе не одно и то же.
K. Serrano et al. / Journal of Nuclear Materials 282 (2000) 137~145
Впрочем, подожду что скажут сами авторы этих тиглей.
Насчёт аниона. Опять возвращаюсь к сути этой темы и характеру возникшего вопроса. Меня интересует будет ли в этом расплаве растворяться металлический иридий в любом виде (порошок, проволока, фольга, куски, что угодно), и, независимо от ответа на этот вопрос, мне нужно либо теоретическое обоснование, либо практический опыт как подтверждение ответу. Условия я старательно описал, могу прояснить если что-то непонятно, но в ответ хочется только конкретики.
Пока с металлическим иридием непонятки, есть вопросы по двум другим вариантам. Я опишу, а вы высказывайтесь.
1. Иридиевый расходуемый анод.
Если анод будет в виде погружённого в расплав небольшого тигля/лодочки, в котором содержится (и пополняется) порошок иридия, будет ли это как-то отличаться для протекания процесса от монолитного иридиевого анода, например проволоки или пластины?
2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
Насчёт стеклографитового тигля. Именно такой применялся во многих экспериментах с электролизом в расплавах NaCl и NaCl/KCl, потому и привлёк внимание. Конкретно вот пример, где стеклографитовый тигель был анодом при электроосаждении урана из UCl3 при 670-710C, и катод тоже был стеклографитовый. Стеклографит и просто графит — это вовсе не одно и то же.
K. Serrano et al. / Journal of Nuclear Materials 282 (2000) 137~145
Впрочем, подожду что скажут сами авторы этих тиглей.
Насчёт аниона. Опять возвращаюсь к сути этой темы и характеру возникшего вопроса. Меня интересует будет ли в этом расплаве растворяться металлический иридий в любом виде (порошок, проволока, фольга, куски, что угодно), и, независимо от ответа на этот вопрос, мне нужно либо теоретическое обоснование, либо практический опыт как подтверждение ответу. Условия я старательно описал, могу прояснить если что-то непонятно, но в ответ хочется только конкретики.
Пока с металлическим иридием непонятки, есть вопросы по двум другим вариантам. Я опишу, а вы высказывайтесь.
1. Иридиевый расходуемый анод.
Если анод будет в виде погружённого в расплав небольшого тигля/лодочки, в котором содержится (и пополняется) порошок иридия, будет ли это как-то отличаться для протекания процесса от монолитного иридиевого анода, например проволоки или пластины?
2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
au> Насчёт аниона. Опять возвращаюсь к сути этой темы и характеру возникшего вопроса. Меня интересует будет ли в этом расплаве растворяться металлический иридий в любом виде (порошок, проволока, фольга, куски, что угодно), и, независимо от ответа на этот вопрос, мне нужно либо теоретическое обоснование, либо практический опыт как подтверждение ответу. Условия я старательно описал, могу прояснить если что-то непонятно, но в ответ хочется только конкретики.
Не будет. Иридий — Википедия
au> Пока с металлическим иридием непонятки, есть вопросы по двум другим вариантам. Я опишу, а вы высказывайтесь.
au> 1. Иридиевый расходуемый анод.
au> Если анод будет в виде погружённого в расплав небольшого тигля/лодочки, в котором содержится (и пополняется) порошок иридия, будет ли это как-то отличаться для протекания процесса от монолитного иридиевого анода, например проволоки или пластины?
Безусловно будет. Для достижения стабильных условий электролиза необходимо поддержание постоянной плотности тока - следовательно площади электрода. При монолитном аноде размером 10 см х 10 см х 1 см расходование 20% массы (1 мм с каждой стороны) приведет к уменьшению площади поверхности на 5,1%. Сфера того же объема будет иметь площадь поверхности 104 см2. Изменение объема на 20% приведет к уменьшению площади до 90 см2, т.е. на 13,5%. При более сложной форме поверхности зависимости будут сложнее. К тому же следует учитывать невозможность обеспечения надежного и одинакового контакта между кускаму иридия в тигле, что приведет к непредсказуемому поведению величины тока электролиза с течением времени и, как следствие, к непредсказуемым свойствам полученного покрытия.
au> 2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
au> Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
Повторю еще раз - IrCl3не единственный хлорид иридия. IrCl4 более устойчив (см. ссылку) и образует с NaCl гексахлориридат Na2IrCl6, растворимый в расплаве NaCl.
Не будет. Иридий — Википедия
au> Пока с металлическим иридием непонятки, есть вопросы по двум другим вариантам. Я опишу, а вы высказывайтесь.
au> 1. Иридиевый расходуемый анод.
au> Если анод будет в виде погружённого в расплав небольшого тигля/лодочки, в котором содержится (и пополняется) порошок иридия, будет ли это как-то отличаться для протекания процесса от монолитного иридиевого анода, например проволоки или пластины?
Безусловно будет. Для достижения стабильных условий электролиза необходимо поддержание постоянной плотности тока - следовательно площади электрода. При монолитном аноде размером 10 см х 10 см х 1 см расходование 20% массы (1 мм с каждой стороны) приведет к уменьшению площади поверхности на 5,1%. Сфера того же объема будет иметь площадь поверхности 104 см2. Изменение объема на 20% приведет к уменьшению площади до 90 см2, т.е. на 13,5%. При более сложной форме поверхности зависимости будут сложнее. К тому же следует учитывать невозможность обеспечения надежного и одинакового контакта между кускаму иридия в тигле, что приведет к непредсказуемому поведению величины тока электролиза с течением времени и, как следствие, к непредсказуемым свойствам полученного покрытия.
au> 2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
au> Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
Повторю еще раз - IrCl3не единственный хлорид иридия. IrCl4 более устойчив (см. ссылку) и образует с NaCl гексахлориридат Na2IrCl6, растворимый в расплаве NaCl.
SkydiVAR> Не будет. Иридий — Википедия
Вики я уже посмотрел. Теперь хочется более авторитетных источников, но пока оставим. Мне в принципе без разницы хлорид там растворяется или металл. Хлор с анода легко будет собрать и тормознуть в поглотителе. С килограмма IrCl3 будет около 360г хлора, в общем-то не проблема.
Теперь хочется более авторитетных источников, но пока оставим. Мне в принципе без разницы хлорид там растворяется или металл. Хлор с анода легко будет собрать и тормознуть в поглотителе. С килограмма IrCl3 будет около 360г хлора, в общем-то не проблема.
SkydiVAR> Безусловно будет. ...
Стабилизация тока для случая с расходуемым анодом трудностей не вызывает, есть много методов на примете. Вообще на данный момент интересен проволочный или ленточный расходуемый анод, автоматически погружаемый в расплав по мере расхода. Таким образом намного легче контролировать процесс по сравнению с растворением хлорида, и исчезает необходимость возни с хлором. Хлорид стоит практически по содержанию металла в нём, как и все металлические формы, так что как минимум два плюса в пользу расходуемого электрода. Ещё стоит сказать что катод видится подвижным для более равномерного осаждения, так что скорость осаждения будет очень даже контролируемой несколькими параметрами (ток, положение анода, движение катода). Ещё один плюс в пользу расходуемого анода — это отсутствие проблем с вариацией концентрации ионов в расплаве. Народ с ураном намучился: у них уран "тонул" в расплаве, концентрация сверху была ниже, и ещё понижалась по мере осаждения, потому то расплав с ураном тяжелее. Три плюса уже...
au>> 2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
au>> Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
SkydiVAR> Повторю еще раз - IrCl3не единственный хлорид иридия. IrCl4 более устойчив (см. ссылку)
А мне какая разница, если я буду сыпать IrCl3? По ссылке на вики лишь подтверждение что он разложится при нагревании расплава выше 800С. Впрочем, что-то я уже охладел к идее с хлоридом, никаких плюсов у него не видно кроме несколько более простого анода. Зато при этом нужен поглотитель для хлора, газоотвод... ну его нафиг, пусть будет расходуемый металлический анод.
Вики я уже посмотрел.
 Теперь хочется более авторитетных источников, но пока оставим. Мне в принципе без разницы хлорид там растворяется или металл. Хлор с анода легко будет собрать и тормознуть в поглотителе. С килограмма IrCl3 будет около 360г хлора, в общем-то не проблема.
Теперь хочется более авторитетных источников, но пока оставим. Мне в принципе без разницы хлорид там растворяется или металл. Хлор с анода легко будет собрать и тормознуть в поглотителе. С килограмма IrCl3 будет около 360г хлора, в общем-то не проблема. SkydiVAR> Безусловно будет. ...
Стабилизация тока для случая с расходуемым анодом трудностей не вызывает, есть много методов на примете. Вообще на данный момент интересен проволочный или ленточный расходуемый анод, автоматически погружаемый в расплав по мере расхода. Таким образом намного легче контролировать процесс по сравнению с растворением хлорида, и исчезает необходимость возни с хлором. Хлорид стоит практически по содержанию металла в нём, как и все металлические формы, так что как минимум два плюса в пользу расходуемого электрода. Ещё стоит сказать что катод видится подвижным для более равномерного осаждения, так что скорость осаждения будет очень даже контролируемой несколькими параметрами (ток, положение анода, движение катода). Ещё один плюс в пользу расходуемого анода — это отсутствие проблем с вариацией концентрации ионов в расплаве. Народ с ураном намучился: у них уран "тонул" в расплаве, концентрация сверху была ниже, и ещё понижалась по мере осаждения, потому то расплав с ураном тяжелее. Три плюса уже...
au>> 2. Инертный нерасходуемый анод и IrCl3 как источник металла в электролите.
au>> Если температура расплава выше чем температура разложения хлорида иридия, и он помещается в расплав, в каком виде он будет находиться в расплаве до приложения напряжения к электродам? Растворится, как хлорид в хлориде?
SkydiVAR> Повторю еще раз - IrCl3не единственный хлорид иридия. IrCl4 более устойчив (см. ссылку)
А мне какая разница, если я буду сыпать IrCl3? По ссылке на вики лишь подтверждение что он разложится при нагревании расплава выше 800С. Впрочем, что-то я уже охладел к идее с хлоридом, никаких плюсов у него не видно кроме несколько более простого анода. Зато при этом нужен поглотитель для хлора, газоотвод... ну его нафиг, пусть будет расходуемый металлический анод.
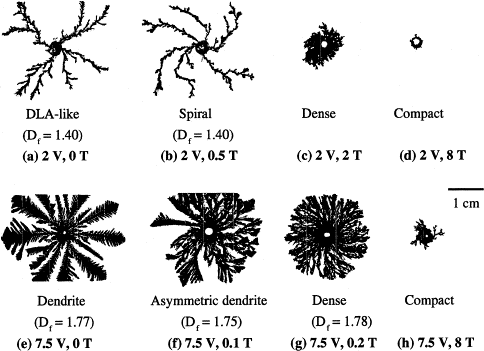
Кстати, что скажете о магнитоэлектролизе в контексте задачи? Народ магнитным полем улучшал структуру осаждаемого металла, очень убедительные снимки: разлапистые дендриты без поля, или куцые дендриты с полем, в роли демонстрации. Вот пример такого дела: Browse Journal - Journal of Applied Physics
au> У Ir3+ потенциал восстановления 1.156В.
Отлично. "Но есть нюансы" (с)М.Жванецкий
1. Это потенциал восстановления до Ir, Ir1+ или Ir2+?
2. Если значение из справочника, то это скорее всего т.н. "стандартный электродный потенциал", т.е. значение, измеренное при нормальных условиях в водном растворе относительно водородного электрода. В расплаве соли значение будет другим и будет меняться в зависимости от температуры, состава электролита и кучи других параметров.
Отлично. "Но есть нюансы" (с)М.Жванецкий
1. Это потенциал восстановления до Ir, Ir1+ или Ir2+?
2. Если значение из справочника, то это скорее всего т.н. "стандартный электродный потенциал", т.е. значение, измеренное при нормальных условиях в водном растворе относительно водородного электрода. В расплаве соли значение будет другим и будет меняться в зависимости от температуры, состава электролита и кучи других параметров.
au> Кстати, что скажете о магнитоэлектролизе в контексте задачи? Народ магнитным полем улучшал структуру осаждаемого металла, очень убедительные снимки: разлапистые дендриты без поля, или куцые дендриты с полем, в роли демонстрации. Вот пример такого дела: Browse Journal - Journal of Applied Physics
Прто магнитоэлектролиз - ничего не скажу, мне сие не ведомо. А ссылка не показывает ничего... :-(
Прто магнитоэлектролиз - ничего не скажу, мне сие не ведомо. А ссылка не показывает ничего... :-(
au> А мне какая разница, если я буду сыпать IrCl3? По ссылке на вики лишь подтверждение что он разложится при нагревании расплава выше 800С. Впрочем, что-то я уже охладел к идее с хлоридом, никаких плюсов у него не видно кроме несколько более простого анода. Зато при этом нужен поглотитель для хлора, газоотвод... ну его нафиг, пусть будет расходуемый металлический анод.
Поддерживаю! Расходуемый иридиевый анод - на мой взгляд идеальный вариант, тем более - электрод стандартной конфигурации (лента, проволока) с автоподачей.
Расходуемый иридиевый анод - на мой взгляд идеальный вариант, тем более - электрод стандартной конфигурации (лента, проволока) с автоподачей.
Поддерживаю!
 Расходуемый иридиевый анод - на мой взгляд идеальный вариант, тем более - электрод стандартной конфигурации (лента, проволока) с автоподачей.
Расходуемый иридиевый анод - на мой взгляд идеальный вариант, тем более - электрод стандартной конфигурации (лента, проволока) с автоподачей.
au>> Кстати, что скажете о магнитоэлектролизе в контексте задачи? Народ магнитным полем улучшал структуру осаждаемого металла, очень убедительные снимки: разлапистые дендриты без поля, или куцые дендриты с полем, в роли демонстрации. Вот пример такого дела: Browse Journal - Journal of Applied Physics
SkydiVAR> Прто магнитоэлектролиз - ничего не скажу, мне сие не ведомо. А ссылка не показывает ничего... :-(
Странно, у меня показывает. В общем вот аннотация:
G. Hinds and J. M. D. Coey, Magnetoelectrolysis of copper, Journal of Applied Physics, volume 83 number 11, 1998
The effect of a uniform static magnetic field on processes occurring at Cu/acidified CuSO4 interfaces is examined by analysis of potentiodynamic polarization curves. The mass transport controlled deposition current is increased by as much as a factor of 2 in a 0.6T field, independent of field direction and electrode orientation. The extent of current enhancement is greatest at low pH (
И ещё одна, посвежее. Суть — с магнитным полем увеличивается ток, уменьшается зернистость, а в целом пока не всё ясно.
A. Bund, S. Koehler, H.H. Kuehnlein, W. Plieth, Magnetic field effects in electrochemical reactions, Electrochimica Acta 49 (2003) 147–152
The influence of an external magnetic field B on the electrochemical behaviour of the systems Cu2+/Cu, Ni2+/Ni, and [IrCl6]2−/[IrCl6]3− has been studied. In the case of Cu depositions in an electrochemical cell with a large ratio of the electrode area and the cell volume the increase of the limiting current density with B can be explained with the interplay of natural convection and the Lorentz force acting on the resulting flowprofile (magneto hydrodynamic or MHD effect). Ni depositions also showan MHD effect as well as a tendency to form more fine grained material in the presence of a magnetic field. The results on the homogeneous redox system [IrCl6]2−/[IrCl6]3− at 50um diameter micro electrodes are in qualitative agreement with recently proposed relationships to describe the influence of a B field on the limiting current density.
SkydiVAR> Прто магнитоэлектролиз - ничего не скажу, мне сие не ведомо. А ссылка не показывает ничего... :-(
Странно, у меня показывает. В общем вот аннотация:
G. Hinds and J. M. D. Coey, Magnetoelectrolysis of copper, Journal of Applied Physics, volume 83 number 11, 1998
The effect of a uniform static magnetic field on processes occurring at Cu/acidified CuSO4 interfaces is examined by analysis of potentiodynamic polarization curves. The mass transport controlled deposition current is increased by as much as a factor of 2 in a 0.6T field, independent of field direction and electrode orientation. The extent of current enhancement is greatest at low pH (
И ещё одна, посвежее. Суть — с магнитным полем увеличивается ток, уменьшается зернистость, а в целом пока не всё ясно.
A. Bund, S. Koehler, H.H. Kuehnlein, W. Plieth, Magnetic field effects in electrochemical reactions, Electrochimica Acta 49 (2003) 147–152
The influence of an external magnetic field B on the electrochemical behaviour of the systems Cu2+/Cu, Ni2+/Ni, and [IrCl6]2−/[IrCl6]3− has been studied. In the case of Cu depositions in an electrochemical cell with a large ratio of the electrode area and the cell volume the increase of the limiting current density with B can be explained with the interplay of natural convection and the Lorentz force acting on the resulting flowprofile (magneto hydrodynamic or MHD effect). Ni depositions also showan MHD effect as well as a tendency to form more fine grained material in the presence of a magnetic field. The results on the homogeneous redox system [IrCl6]2−/[IrCl6]3− at 50um diameter micro electrodes are in qualitative agreement with recently proposed relationships to describe the influence of a B field on the limiting current density.
Это сообщение редактировалось 24.07.2007 в 15:31
au> The mass transport controlled deposition current is increased by as much as a factor of 2 in a 0.6T field, independent of field direction and electrode orientation. The extent of current enhancement is greatest at low pH (<1), where it is associated with diffusional rather than migrational transport of the copper ions.
au> Суть — с магнитным полем увеличивается ток, уменьшается зернистость, а в целом пока не всё ясно.
Идея, конечно, интересная... Вот только 0,6 Тесла - это довольно сильное поле. А кроме того - влияние на процесс описано как МГД-эффект, если я правильно понял. Т.е. это влияние существенно зависит от состава электролита, от состава и структуры промежуточных комплексов, образующихся при электролизе, рН и т.д. Опять же, электролиз в водном растворе... Не знаю... Я точно ничего умного по этому поводу не скажу.
Вообще, по поводу иридия могу только предложить сходить в библиотеку. Ссылочки я нашел, а вот самих книжек в инете найти не удалось.
Ливингстон С., Химия рутения, родия, палладия, осмия, иридия, платины, М., Мир, 1978
Синицын Н. М., Большаков К. А. и др. Химия платиновых металлов. -М.: изд-во МИТХТ ак. Менделеева, 1987. 85с.
// www.chem.msu.su
http://kristall.lan.krasu.ru/Education/Aurum/aurum.html
http://journal.issep.rssi.ru/...
au> Суть — с магнитным полем увеличивается ток, уменьшается зернистость, а в целом пока не всё ясно.
Идея, конечно, интересная... Вот только 0,6 Тесла - это довольно сильное поле. А кроме того - влияние на процесс описано как МГД-эффект, если я правильно понял. Т.е. это влияние существенно зависит от состава электролита, от состава и структуры промежуточных комплексов, образующихся при электролизе, рН и т.д. Опять же, электролиз в водном растворе... Не знаю... Я точно ничего умного по этому поводу не скажу.
Вообще, по поводу иридия могу только предложить сходить в библиотеку. Ссылочки я нашел, а вот самих книжек в инете найти не удалось.
Ливингстон С., Химия рутения, родия, палладия, осмия, иридия, платины, М., Мир, 1978
Синицын Н. М., Большаков К. А. и др. Химия платиновых металлов. -М.: изд-во МИТХТ ак. Менделеева, 1987. 85с.
Портал фундаментального химического образования России. Наука. Образование. Технологии.
Химическая информация России. Наука. Образование. Технологии.// www.chem.msu.su
http://kristall.lan.krasu.ru/Education/Aurum/aurum.html
http://journal.issep.rssi.ru/...
Это сообщение редактировалось 24.07.2007 в 16:28
MIKLE>> стеклоуглерод... гм...
au> HTW Germany
в нас раньше вроде делии в нии графит, но счас оно здохло..
au> А по теме что скажете? Ждал, если честно.
а хз... даже не знаю что и сказать... если подорпть условия-наверно можно избирательно выделять... а в чём лопата то? в том что иридий?
зы по результатам второй страницы-это скорее нанесение покрытия одновременно с рафинированием. суём в расплав губку и деталюшку, даём ток, получаем хорошее покрытие из чистого ириди...
au> HTW Germany
в нас раньше вроде делии в нии графит, но счас оно здохло..
au> А по теме что скажете? Ждал, если честно.

а хз... даже не знаю что и сказать... если подорпть условия-наверно можно избирательно выделять... а в чём лопата то? в том что иридий?
зы по результатам второй страницы-это скорее нанесение покрытия одновременно с рафинированием. суём в расплав губку и деталюшку, даём ток, получаем хорошее покрытие из чистого ириди...
Это сообщение редактировалось 24.07.2007 в 16:51
Ну вот, авторы говорят что ни галогениды, ни хлор (спросил до 1000С) их стеклографиту совсем не страшны. Так что тигель может быть анодом, а на дно ему можно порошок подсыпать (или проволоку равномерно нарубленную) для грубой регуляции тока при неизменном напряжении, а тонко ток регулировать можно небольшим изменением напряжения. Так что с электродами тема раскрыта. 
SkydiVAR:
Спасибо за усилия, в библиотеку я уже "сходил", книги и периодика есть. Ниже иллюстрация как растут кристаллы без поля и с разной силой поля. Это цинк рос из сульфата.
Ниже иллюстрация как растут кристаллы без поля и с разной силой поля. Это цинк рос из сульфата.
MIKLE:
Лопата в нескольких моментах. Во-1 с иридием просто так не поиграешься и не потренируешься ввиду его ненулевой стоимости. Во-2 это усугубляется его невосприимчивостью к нормальной химии, из-за чего появляютя расплавы солей с ненулевой стоимостью нужного для этого оборудования. Всё нужно заблаговременно и тщательно выяснить, и только потом браться, а не наоборот, как это принято.
Во-2 это усугубляется его невосприимчивостью к нормальной химии, из-за чего появляютя расплавы солей с ненулевой стоимостью нужного для этого оборудования. Всё нужно заблаговременно и тщательно выяснить, и только потом браться, а не наоборот, как это принято. 
Рафинировать как раз ничего не нужно — всё готовится в чистом виде. С осаждением есть нюансы, смотрите картинку ниже.

SkydiVAR:
Спасибо за усилия, в библиотеку я уже "сходил", книги и периодика есть.
 Ниже иллюстрация как растут кристаллы без поля и с разной силой поля. Это цинк рос из сульфата.
Ниже иллюстрация как растут кристаллы без поля и с разной силой поля. Это цинк рос из сульфата.MIKLE:
Лопата в нескольких моментах. Во-1 с иридием просто так не поиграешься и не потренируешься ввиду его ненулевой стоимости.
 Во-2 это усугубляется его невосприимчивостью к нормальной химии, из-за чего появляютя расплавы солей с ненулевой стоимостью нужного для этого оборудования. Всё нужно заблаговременно и тщательно выяснить, и только потом браться, а не наоборот, как это принято.
Во-2 это усугубляется его невосприимчивостью к нормальной химии, из-за чего появляютя расплавы солей с ненулевой стоимостью нужного для этого оборудования. Всё нужно заблаговременно и тщательно выяснить, и только потом браться, а не наоборот, как это принято. 
Рафинировать как раз ничего не нужно — всё готовится в чистом виде. С осаждением есть нюансы, смотрите картинку ниже.
Прикреплённые файлы:
Это сообщение редактировалось 24.07.2007 в 18:54
au> Ну вот, авторы говорят что ни галогениды, ни хлор (спросил до 1000С) их стеклографиту совсем не страшны. Так что тигель может быть анодом, а на дно ему можно порошок подсыпать (или проволоку равномерно нарубленную) для грубой регуляции тока при неизменном напряжении, а тонко ток регулировать можно небольшим изменением напряжения. Так что с электродами тема раскрыта. 
Раскрыта. Однако для обеспечения равномерности концентрации иридия в объеме расплава необходимо обеспечить его циркуляцию в ванне (тигле). Иначе весь иридий будет "лежать" на дне - и металл, и раствор гексахлориридатов в NaCl. А концентрация этих пресловутых гексахлориридатов в верхней части тигля будет низкой. Вспомните Ваш пост насчет урана.
Вообще, если тигель сделать катодом, например, придав ему форму того же сопла и заизолировав часть поверхности (там, где предполагаются отверстия) керамикой или стеклом, а ленточный/проволочный анод, а лучше - десяток-другой таких анодов, равномерно размещенных по поверхности тигля подавать в тигель сверху - то все выглядит еще проще.

Раскрыта. Однако для обеспечения равномерности концентрации иридия в объеме расплава необходимо обеспечить его циркуляцию в ванне (тигле). Иначе весь иридий будет "лежать" на дне - и металл, и раствор гексахлориридатов в NaCl. А концентрация этих пресловутых гексахлориридатов в верхней части тигля будет низкой. Вспомните Ваш пост насчет урана.
Вообще, если тигель сделать катодом, например, придав ему форму того же сопла и заизолировав часть поверхности (там, где предполагаются отверстия) керамикой или стеклом, а ленточный/проволочный анод, а лучше - десяток-другой таких анодов, равномерно размещенных по поверхности тигля подавать в тигель сверху - то все выглядит еще проще.
Про циркуляцию расплава я уже думал. Чувствую что тут не хватает знаний: ведь ионы движутся полем, а не только диффузией, так что должны подниматься и снизу. Так?
Но можно и циркуляцию устроить, дело нехитрое в проводящей среде.
Катодом тигель быть не сможет, форма не позволяет. Более того, если с первого раза не получится, захочется повторить, и потому и тигель и электроды видятся неодноразовыми, ведь изготовление катода будет небесплатным даже с сегодняшними обрабатывающими центрами и мягким материалом (графитом). Кстати, а чем можно изолировать в таком расплаве, чтобы изолятор никак не растворялся и не загадил всё? Я думал про BN, очень удобная штука для этого, как графит, но не знаю как он себя поведёт там. Да и пористый он, набьётся в него иридий, и доставай его потом оттуда. И не такой уж BN нейтральный при таких высоких температурах, хотя это как раз можно испытать. Хотя есть BN горячего прессования, он вроде ничего. Изолирующие накладки-маски неизбежно понадобятся, это всяко легче и дешевле, чем потом ковырять фигурные дырки в иридии.
С анодом простота не главное, главное — качество. Плотность тока при прочих равных пропорциональна (т.е. индикатор, потому что ток — это направленное движение ионов) скорости осаждения. Толщина слоя должна быть известной и управляемой, поэтому анод мне (как вариант) видится не просто висящим в тигле электродом, а точно управляемым в 2D подвижным электродом, чтобы можно было контролировать плотность тока для небольшого участка катода. И вообще всё это хозяйство видится под управлением программы с автоматическим контролем физических параметров процесса, и рассчитанным контролируемым движением электродов. Таким образом есть хорошие шансы что изделие получится как задумано и с минимальным расходом металла.
Но можно и циркуляцию устроить, дело нехитрое в проводящей среде.
Катодом тигель быть не сможет, форма не позволяет. Более того, если с первого раза не получится, захочется повторить, и потому и тигель и электроды видятся неодноразовыми, ведь изготовление катода будет небесплатным даже с сегодняшними обрабатывающими центрами и мягким материалом (графитом). Кстати, а чем можно изолировать в таком расплаве, чтобы изолятор никак не растворялся и не загадил всё? Я думал про BN, очень удобная штука для этого, как графит, но не знаю как он себя поведёт там. Да и пористый он, набьётся в него иридий, и доставай его потом оттуда. И не такой уж BN нейтральный при таких высоких температурах, хотя это как раз можно испытать. Хотя есть BN горячего прессования, он вроде ничего. Изолирующие накладки-маски неизбежно понадобятся, это всяко легче и дешевле, чем потом ковырять фигурные дырки в иридии.
С анодом простота не главное, главное — качество. Плотность тока при прочих равных пропорциональна (т.е. индикатор, потому что ток — это направленное движение ионов) скорости осаждения. Толщина слоя должна быть известной и управляемой, поэтому анод мне (как вариант) видится не просто висящим в тигле электродом, а точно управляемым в 2D подвижным электродом, чтобы можно было контролировать плотность тока для небольшого участка катода. И вообще всё это хозяйство видится под управлением программы с автоматическим контролем физических параметров процесса, и рассчитанным контролируемым движением электродов. Таким образом есть хорошие шансы что изделие получится как задумано и с минимальным расходом металла.
au> это усугубляется его невосприимчивостью к нормальной химии
Да нормальная у него химия. И электролизом из водного раствора осаждается. Только пока не нашли водный электролит, который бы давал прочное покрытие.
Для примера, какие хитрые электролиты приходится изобретать, чтобы получить слой металла нужного качества, приведу электролиты для палладирования:
хлористый палладий
хлористый аммоний
малеиновый ангидрид
хинолин
вода
хлористый палладий
гидрофосфат натрия
гидрофосфат аммония
бензойная кислота
вода
Вот для золочения:
дицианоаурат калия
калий дигидроцитрат
сульфат никеля
лимонная кислота
вода
дицианоаурат калия
цианистый калий
карбонат калия
трёхокись сурьмы
Для осаждения меди тоже непростые электролиты, хотя казалось бы, чего уж проще - медь осадить.
Цианистая медь
цианистый натрий
едкий натр
сегнетовая соль
вода
Цианистая медь
цианистый натрий
едкий натр
роданистый аммоний
виннокислый натрий
сернокислый марганец
вода
Как видно, каждый электролит кроме соли металла содержит несколько "ненужных" компонентов. Без них электролиз тоже идёт, но металл осаждается в виде рыхлого порошка или непрочной пористой плёнки.
Поэтому мне кажется малореальным решение вопроса, вынесенного в заголовок темы, силами меньшими, чем группой опытных специалистов-гальваников. Впрочем, чудеса бывают.
Да нормальная у него химия. И электролизом из водного раствора осаждается. Только пока не нашли водный электролит, который бы давал прочное покрытие.
Для примера, какие хитрые электролиты приходится изобретать, чтобы получить слой металла нужного качества, приведу электролиты для палладирования:
хлористый палладий
хлористый аммоний
малеиновый ангидрид
хинолин
вода
хлористый палладий
гидрофосфат натрия
гидрофосфат аммония
бензойная кислота
вода
Вот для золочения:
дицианоаурат калия
калий дигидроцитрат
сульфат никеля
лимонная кислота
вода
дицианоаурат калия
цианистый калий
карбонат калия
трёхокись сурьмы
Для осаждения меди тоже непростые электролиты, хотя казалось бы, чего уж проще - медь осадить.
Цианистая медь
цианистый натрий
едкий натр
сегнетовая соль
вода
Цианистая медь
цианистый натрий
едкий натр
роданистый аммоний
виннокислый натрий
сернокислый марганец
вода
Как видно, каждый электролит кроме соли металла содержит несколько "ненужных" компонентов. Без них электролиз тоже идёт, но металл осаждается в виде рыхлого порошка или непрочной пористой плёнки.
Поэтому мне кажется малореальным решение вопроса, вынесенного в заголовок темы, силами меньшими, чем группой опытных специалистов-гальваников. Впрочем, чудеса бывают.
Serge77> Поэтому мне кажется малореальным решение вопроса, вынесенного в заголовок темы, силами меньшими, чем группой опытных специалистов-гальваников. Впрочем, чудеса бывают.
Этот вопрос давно решён ( iridium plating - Google Patents ), всё давно опубликовано и буднично применяется в промышленности. В заголовок темы вынесен тоже решённый вопрос, только недостаточно подробно опубликованный. В расплаве и с иридиевым анодом всё как минимум делается весьма прозаично, но есть нюансы с качеством металла, с источником металла, и прочее мне интересное, что тут и обсуждается.
Повторяю: давайте придерживаться конкретной темы.
Этот вопрос давно решён ( iridium plating - Google Patents ), всё давно опубликовано и буднично применяется в промышленности. В заголовок темы вынесен тоже решённый вопрос, только недостаточно подробно опубликованный. В расплаве и с иридиевым анодом всё как минимум делается весьма прозаично, но есть нюансы с качеством металла, с источником металла, и прочее мне интересное, что тут и обсуждается.
Повторяю: давайте придерживаться конкретной темы.
au> Этот вопрос давно решён ( iridium plating - Google Patents ), всё давно опубликовано и буднично применяется в промышленности
Тогда зачем что-то изобретать? Почему не применить готовое описанное?
Тогда зачем что-то изобретать? Почему не применить готовое описанное?
au> Про циркуляцию расплава я уже думал. Чувствую что тут не хватает знаний: ведь ионы движутся полем, а не только диффузией, так что должны подниматься и снизу. Так?
Так. Только линейная скорость движения ионов весьма невелика. Без перемешивания - фигня получится.
au> Кстати, а чем можно изолировать в таком расплаве, чтобы изолятор никак не растворялся и не загадил всё?
А почему бы и не аморфным кварцем, осажденным по CVD-технологии?
Так. Только линейная скорость движения ионов весьма невелика. Без перемешивания - фигня получится.
au> Кстати, а чем можно изолировать в таком расплаве, чтобы изолятор никак не растворялся и не загадил всё?
А почему бы и не аморфным кварцем, осажденным по CVD-технологии?
au> Увы, поволочный и ленточный анод отменяется, потому что стоит это в 15-20 раз дороже порошка... Так что придётся думать.  Начинаю понимать г-на Щетковского...
Начинаю понимать г-на Щетковского...
А как иридий прессуется? Может этот порошок спрессовать/запечь в компактный анод?
 Начинаю понимать г-на Щетковского...
Начинаю понимать г-на Щетковского...А как иридий прессуется? Может этот порошок спрессовать/запечь в компактный анод?
Copyright © Balancer 1997..2019
Создано 20.07.2007
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
Создано 20.07.2007
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
 SkydiVAR
SkydiVAR

 инфо
инфо инструменты
инструменты
 MIKLE
MIKLE

 Serge77
Serge77

